近期,南方科技大学材料科学与工程系副教授任富增课题组在生物医用骨科植入材料方面取得一系列研究进展,在国际知名期刊连续发表5篇论文。
由于人口老龄化、意外事故及骨组织疾病等原因,每年有不计其数的骨受损患者需要接受手术治疗,骨修复生物材料及植入器械是保障人类健康的重要手段。因此,开发用于骨组织修复、替代或促进骨组织再生的新材料至关重要,在挽救数以万计的重病患者、提高患者生活质量和降低医疗成本等方面发挥着重要作用。
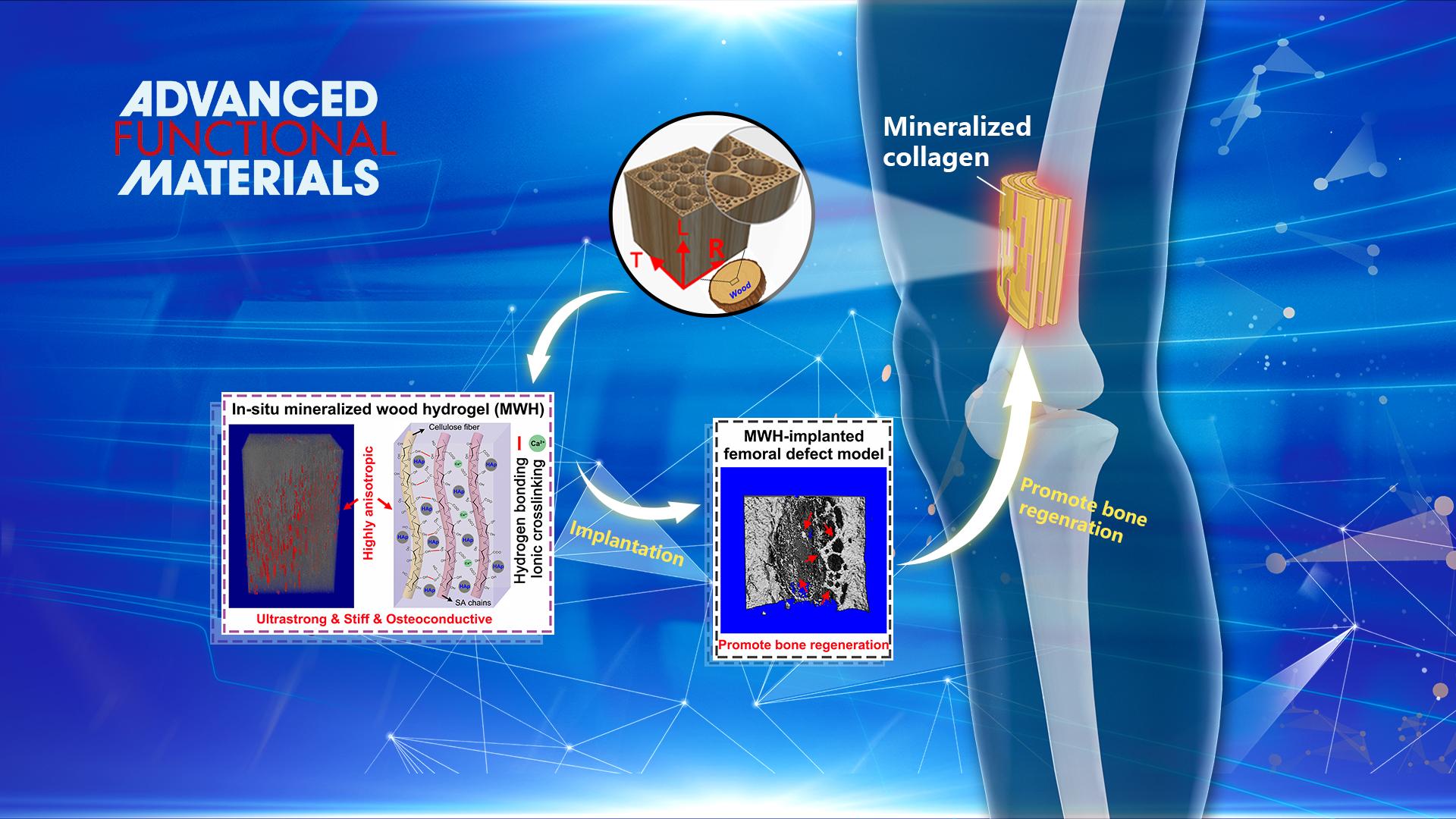
天然骨具有非常精巧的各向异性结构。在纳米尺度下,羟基磷灰石(HA)晶体在胶原蛋白纤维束间隙有序分布,再经层层组装得到多级有机/无机复合结构。这种精细而有序的定向结构赋予了骨组织优异的力学性能和生物功能。如何在人工材料中实现这种复杂的精细分级结构和生物功能,对设计与天然骨力学和生物适配的骨修复材料,改善植入后的骨整合性具有重要的科学意义和应用价值。与天然骨相似,木材是一种天然的各向异性多级组装材料。定向排列的纤维素纤维充当骨架,木质素与半纤维素充当粘合剂,共同构成了木材“钢筋混凝土”式的微观结构,使木材具备超强的力学性能。受天然骨和木材各向异性多级结构启发,研究团队开发了一种“从木头到人工骨”的仿生设计策略,首先对天然木材进行脱木质素处理得到多孔的木质纤维素模板,再利用真空浸润法将海藻酸盐溶液浸渍到模板孔隙中,交联后原位沉积HA纳米晶,得到一种高取向度的HA-木材-水凝胶复合材料。研究结果表明,该复合材料沿纤维取向的拉伸强度高达67.8 MPa,压缩强度达39.5 MPa,超过了目前大多数的强韧水凝胶。在微观结构上,HA纳米颗粒有序沉积在纤维骨架间隙,模拟了骨组织中胶原纤维和HA晶粒的有机/无机复合结构和成分,成功诱导细胞定向粘附,促进细胞骨向分化。动物植入实验结果表明,这种复合支架材料能显著加速支架界面处的新骨生成,并诱导新骨向支架内生长,从而提高了支架整体的骨整合性。该研究成果以“Bioinspired Highly Anisotropic, Ultrastrong and Stiff, and Osteoconductive Mineralized Wood Hydrogel Composites for Bone Repair”为题发表在Advanced Functional Materials。
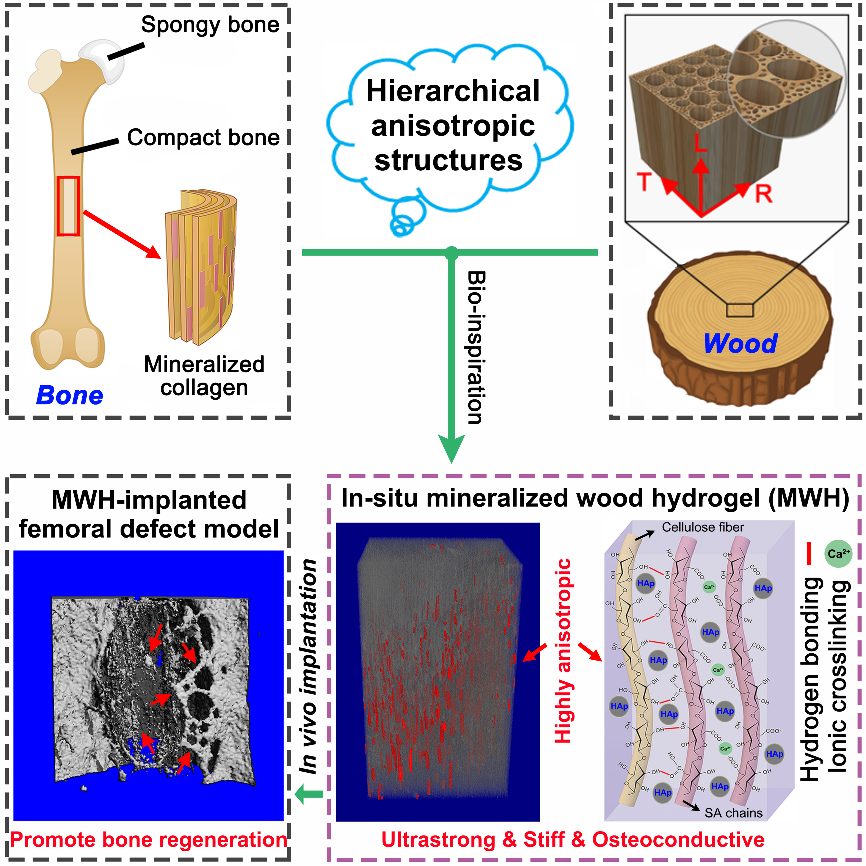
图1. HA纳米晶/海藻酸盐水凝胶/木材复合材料的仿生设计策略及其在骨修复中的潜在应用
成骨性能差和植入体相关的感染是造成骨科植入体失效的重要原因。在植入体表面实现促进成骨和抗细菌感染的有机统一是当前骨科植入材料表面改性的巨大挑战。研究团队在前期医用钛表面构筑高分辨率、形貌尺寸可控的拓扑结构并利用材料基因组的方法高通量筛选了对促进细胞成骨分化的表面拓扑结构和几何尺寸 (ACS Appl. Mater. Interfaces 2019, 11, 47, 43888–43901)的研究基础上,为提高骨诱导性和抗菌性,在优化筛选的拓扑钛表面进一步沉积了金属钽和钽铜纳米双层薄膜,并系统研究了其对细胞增殖分化、基因表达的影响及抗菌性能。结果表明,表面微纳拓扑结构可以有效地调控细胞形态和骨向分化;钽和钽铜薄膜具有良好的细胞相容性,适合于细胞的粘附、增殖和分化,并具有抗细菌感染功能。体内植入实验进一步证实了表面微纳拓扑结构和钽铜双层薄膜的协同效应可显著诱导成骨并抗细菌感染作用。本研究对医用金属表面生物功能设计具有重要意义。该研究成果以“The synergy of topographical micropatterning and Ta|TaCu bilayered thin film on titanium implants enables dual-functions of enhanced osteogenesis and anti-infection”为题发表在Advanced Healthcare Materials。
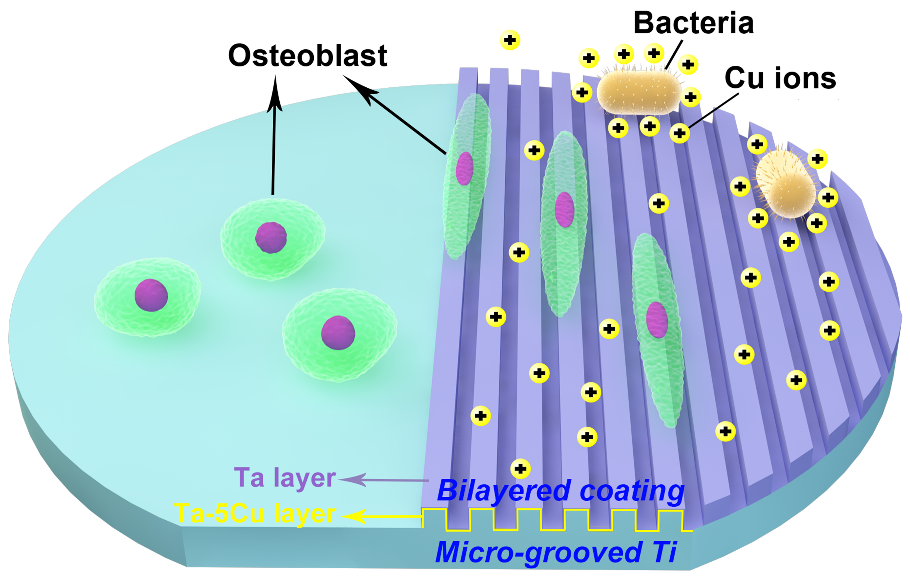
图2. 微纳拓扑结构与Ta|TaCu双层纳米薄膜的协同效应对细胞接触引导作用和抗菌机理示意图
在可降解金属支架领域,铁具有优异的力学性能,但其降解速率过慢;锌具有适中的降解速率,且其降解产物可被吸收。然而,与铁相比,锌的力学强度低(尤其为三维多孔结构时),而且多孔锌存在制备困难、体内降解机制仍不清楚等问题,从而限制了其在骨修复材料中的应用。基于此,研究团队通过模板辅助电沉积技术制备出一种具有核-壳结构的Fe@Zn多孔支架,其孔隙结构和力学性能均与天然松质骨类似,且具有优异的抗菌性和良好的促进骨修复作用。另外,利用聚焦离子束(FIB)-透射电镜(TEM)技术在纳米尺度上分析了多孔锌在体内的降解产物,阐明了其降解机制。该研究证明了Fe@Zn多孔支架作为可降解骨科植入体的可行性,并提供了锌体内降解产物的直接证据。该研究成果以“Cancellous bone-like porous Fe@Zn scaffolds with core-shell-structured skeletons for biodegradable bone implants”为题发表在Acta Biomaterialia。
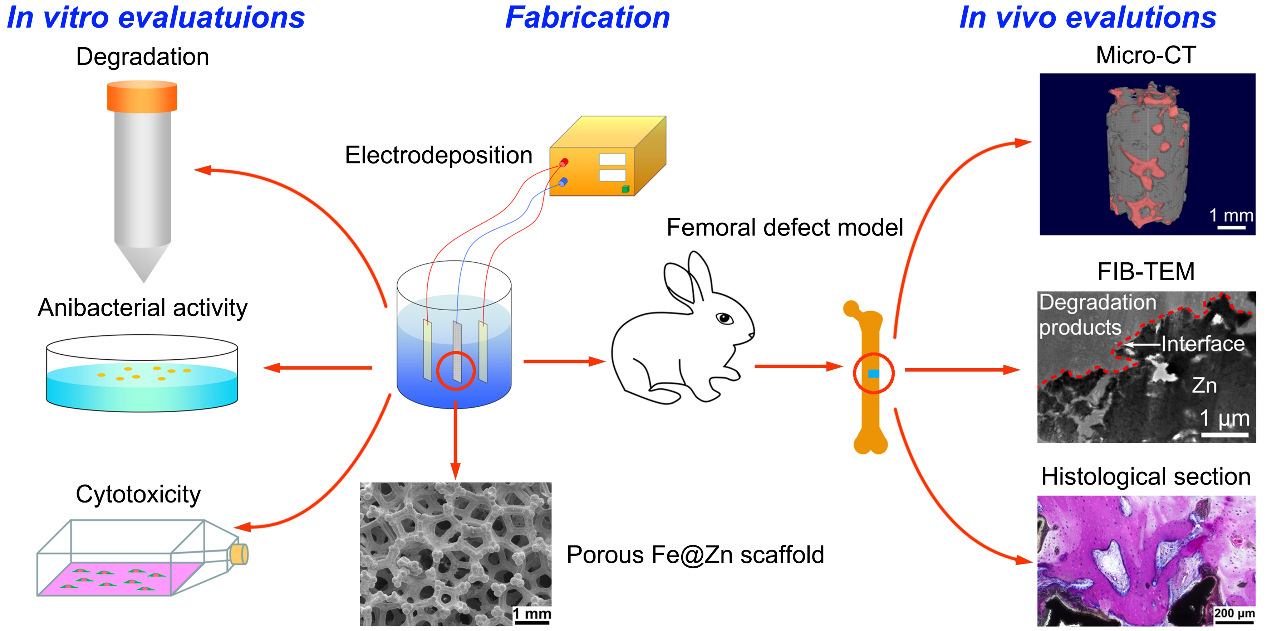
图3. Fe@Zn支架的制备、体内、体外研究示意图
Ti-12Mo-6Zr-2Fe合金是近年来广受推崇的一种生物医用β钛合金,作为骨修复材料具有巨大的应用潜力,但其力学性能与天然骨骼不匹配,容易造成应力屏蔽效应。骨修复金属支架材料不仅需要具备接近人体骨的低弹性模量,亦需要较高的屈服强度以及一定的延展性,以应对植入体长期服役过程中的循环疲劳冲击。因此,如何在维持低模量的同时获得高屈服强度成为了一大科学难题。而且,这类β钛合金材料由于含有大量的难熔元素,传统工艺通常需要长时间的均匀化处理以解决组织均匀性的问题,其低切削速率也给个性化植入材料的加工带来了挑战。3D打印技术近年在骨科植入材料的个性化定制方面展现了显著的优越性。研究团队采用粉末床激光3D打印技术,结合低成本的原位合金化方法成功制备了组织均匀的Ti-12Mo-6Zr-2Fe合金。通过调控成型参数以及后处理工艺,控制成型件的显微组织(包括晶粒的择优取向、晶格缺陷以及析出相组成),获得了优异的力学性能,同时兼具高强度和低模量,为高性能生物医用钛合金植入材料的制备提供了一个新的选择,对于发展高强度3D打印β钛合金材料具有重要的意义。该研究成果以“A high strength and low modulus metastable β Ti-12Mo-6Zr-2Fe alloy fabricated by laser powder bed fusion in-situ alloying”为题发表在Additive Manufacturing。
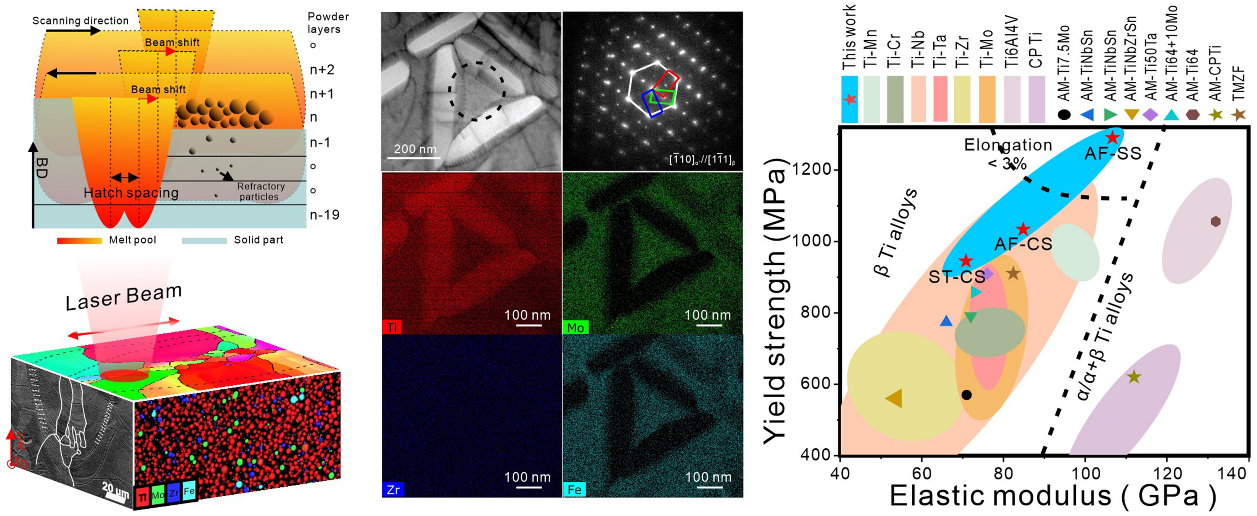
图4. 原位合金化粉末床激光3D打印 β Ti-12Mo-6Zr-2Fe合金的加工示意图、显微组织以及力学性能
难熔金属铌(Nb) 具有抗腐蚀、耐磨损、延展性较高、易于成型、磁化率低、与核磁共振成像兼容等优点,是一种潜在的骨科植入材料。然而,传统粗晶组织的铌屈服强度低、缺乏抗菌性,而且熔点高、易于和氧发生反应,制造成本和难度较高,限制了其在骨科植入材料的广泛应用。基于此,研究团队通过机械合金化和放电等离子体烧结(SPS)技术制备了纳米结构的Nb-5 at.% Ag合金。相比于纯Nb,Nb-5 at% Ag合金的压缩强度(1486 Mpa)和塑性(35%)显著提高。Nb基体上析出的Ag第二相不仅大幅提高了合金的摩擦学性能,而且赋予了Nb很强的抗菌性(抗菌率达99%)。动物体内植入实验也证实了该合金良好的生物相容性、抗感染功能和骨整合性。这种力学性能、耐腐蚀性、生物相容性及抗菌性良好的Nb基纳米结构合金有望成为一种新型的骨科植入金属材料。该研究成果以“A high strength, wear and corrosion-resistant, antibacterial and biocompatible Nb-5 at.% Ag alloy for dental and orthopedic implants”为题发表在Journal of Materials Science & Technology。
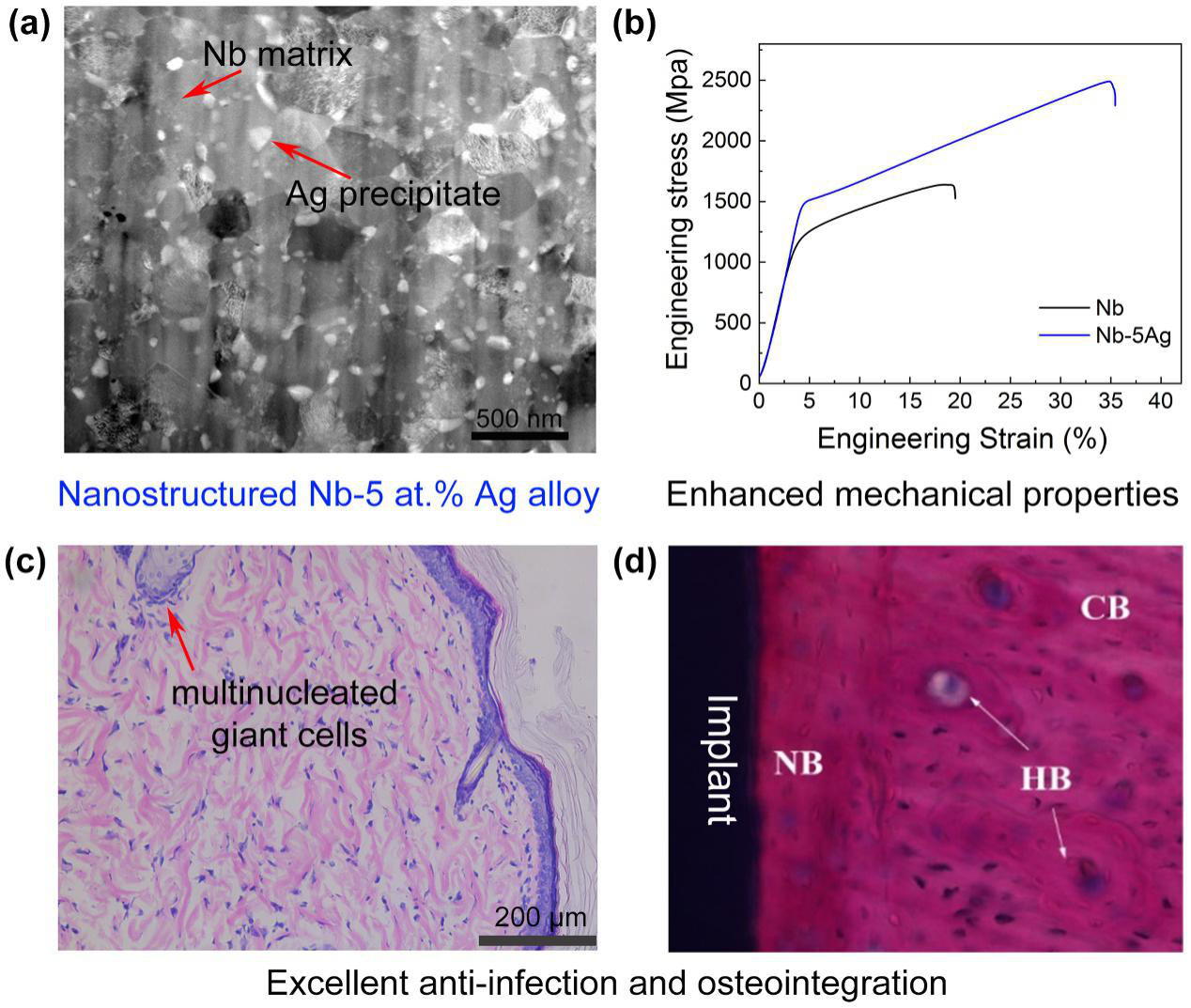
图5. 纳米结构Nb-5 at% Ag合金呈现优异的力学、抗感染和骨整合性能
以上系列研究工作均以南方科技大学为第一通讯单位,任富增为论文通讯作者。主要贡献者有:材料科学与工程系、前沿与交叉科学研究院研究助理教授王晓飞,材料科学与工程系研究助理教授方驹、何进,博士生朱明余、段然曦,科研助理万天、2012级本科生储康杰;论文的合作者包括南方科技大学讲席教授赵予生,西南交通大学教授鲁雄,五邑大学助理教授叶冬冬,伯明翰大学教授Moataz M. Attallah 等。以上研究工作得到了国家重点研发计划、广东省自然科学基金、深圳市基础研究项目的资助以及南方科技大学分析测试中心成像平台、微纳平台以及实验动物中心的大力支持。
相关论文链接:
论文链接:https://doi.org/10.1002/adfm.202010068
论文链接:https://doi.org/10.1002/adhm.202002020
论文链接:https://doi.org/10.1016/j.actbio.2020.11.032
论文链接:https://doi.org/10.1016/j.addma.2020.101708
论文连接:https://doi.org/10.1016/j.jmst.2020.11.049
供稿单位:材料科学与工程系
编辑:程雯璟
主图设计:丘妍






